Cục Quản lý Dược (Bộ Y tế) vừa công bố danh sách 46 công ty nước ngoài thuộc 12 quốc gia có thuốc vi phạm chất lượng, buộc phải tiếp tục tiền kiểm 100% đối với tất cả các lô thuốc nhập khẩu vào Việt Nam. Đây là danh sách thuộc đợt công bố lần thứ 42 cho thấy, tình trạng vi phạm chất lượng thuốc của một số nhà sản xuất nước ngoài vẫn chưa được khắc phục triệt để.
Theo danh sách mới công bố, Ấn Độ tiếp tục là quốc gia chiếm số lượng doanh nghiệp vi phạm nhiều nhất. Nhiều công ty đã bị đưa vào diện giám sát từ giai đoạn 2013–2015 đến nay nhưng vẫn chưa đủ điều kiện để được rút khỏi danh sách. Các doanh nghiệp điển hình gồm: ACI Pharma, All Serve Healthcare, Altomega Drugs, AMN Life Science, Chemfar Organics, Elegant Drugs, Euro Healthcare, Fine Pharmachem, Mediwin Pharmaceuticals…
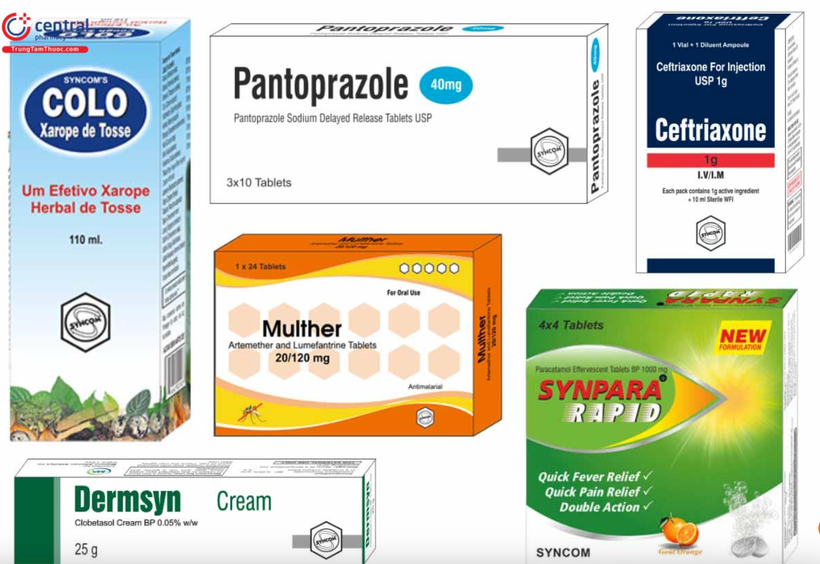
Những cái tên này không chỉ xuất hiện một lần mà được công bố lặp đi lặp lại trong nhiều đợt khác nhau, phản ánh tình trạng vi phạm kéo dài và mang tính hệ thống. Đáng chú ý, một số nhà sản xuất thậm chí vi phạm ở cả khâu tiền kiểm và hậu kiểm như AMN Life Science, Medico Remedies, Syncom Formulations, Minimed Laboratories hay Marksans Pharma.
Trong đó, Syncom Formulations được ghi nhận có tới 8 lần vi phạm mức 2 và 4 lần vi phạm mức 3, tổng cộng 12 lần vi phạm, xuất hiện gần như xuyên suốt ở các đợt công bố. Minimed Laboratories cũng có 6 lần vi phạm mức 2 và 2 lần vi phạm mức 3. Các công ty như Marksans Pharma, Medico Remedies hay AMN Life Science đều có số lần vi phạm vượt trội so với phần lớn doanh nghiệp khác, cho thấy việc kiểm soát chất lượng tại các cơ sở này chưa có chuyển biến rõ rệt.
Không chỉ tập trung ở Ấn Độ, danh sách còn ghi nhận nhiều công ty đến từ Bangladesh, Trung Quốc, Indonesia, Hàn Quốc, Pakistan, Mỹ, Italy và Romania tiếp tục nằm trong diện giám sát. Reman Drug Laboratories (Bangladesh), CSPC Zhongnuo (Trung Quốc), PT. Merck Tbk (Indonesia), Crown Pharm và Yuyu Inc. (Hàn Quốc) đã từng bị công bố vi phạm từ những đợt rất sớm nhưng vẫn chưa đáp ứng yêu cầu để được dỡ bỏ biện pháp tiền kiểm.
Một số doanh nghiệp tại Mỹ như ADH Health Products hay Robinson Pharma cũng tiếp tục xuất hiện trong danh sách, cho thấy tình trạng vi phạm chất lượng thuốc không chỉ xảy ra tại các quốc gia đang phát triển mà còn hiện diện ở những nước có nền công nghiệp dược phẩm lớn. Điểm chung của 46 công ty là đều có thuốc nhập khẩu vào Việt Nam không đạt tiêu chuẩn chất lượng, buộc phải áp dụng cơ chế giám sát nghiêm ngặt hơn trước khi sản phẩm được phép lưu hành.
Theo quy định hiện hành, doanh nghiệp có thuốc vi phạm chất lượng phải thực hiện tiền kiểm đối với tất cả các lô thuốc nhập khẩu trong thời hạn từ 6–12 tháng, tùy theo mức độ vi phạm. Chỉ khi kết thúc thời gian giám sát và không phát sinh thêm vi phạm mới, công ty mới đủ điều kiện để được xem xét rút khỏi danh sách.
Tuy nhiên, việc toàn bộ 46 doanh nghiệp trong danh sách đợt 42 vẫn tiếp tục bị áp dụng biện pháp tiền kiểm cho thấy phần lớn các công ty này chưa đáp ứng yêu cầu theo quy định. Một số doanh nghiệp có lịch sử vi phạm kéo dài nhiều năm, khiến thời gian giám sát liên tục bị gia hạn. Một số khác trong thời gian bị theo dõi vẫn chưa chứng minh được sự cải thiện rõ rệt về chất lượng sản phẩm.
Bên cạnh danh sách vi phạm, Cục Quản lý Dược cũng cho biết, đã có 98 công ty từ 16 quốc gia được rút khỏi danh sách giám sát sau khi hoàn thành đầy đủ thời gian tiền kiểm và không phát sinh thêm vi phạm. Điều này cho thấy cơ chế giám sát không mang tính “đóng khung” lâu dài mà phụ thuộc vào việc doanh nghiệp có thực sự khắc phục và tuân thủ các tiêu chuẩn chất lượng hay không.
Tuy nhiên, đợt công bố lần thứ 42 cũng đồng thời phản ánh một thực trạng đáng lo ngại, vẫn còn một nhóm doanh nghiệp nước ngoài liên tục tái diễn vi phạm bất chấp các biện pháp quản lý đã được áp dụng trong thời gian dài. Điều này đặt ra yêu cầu phải tiếp tục duy trì phương thức tiền kiểm nghiêm ngặt, thậm chí tăng cường hơn nữa việc giám sát đối với các lô thuốc nhập khẩu từ những đơn vị này.
Trong bối cảnh Việt Nam vẫn phải nhập khẩu một lượng lớn thuốc thành phẩm và nguyên liệu từ nhiều thị trường khác nhau, việc áp dụng cơ chế tiền kiểm 100% các lô thuốc của doanh nghiệp vi phạm được xem là “hàng rào kỹ thuật” cần thiết nhằm bảo đảm an toàn cho người bệnh. Việc công bố danh sách định kỳ cũng giúp các cơ sở y tế, doanh nghiệp nhập khẩu và phân phối thuốc chủ động hơn trong việc lựa chọn nguồn cung, hạn chế tối đa nguy cơ thuốc không đạt tiêu chuẩn lọt vào hệ thống điều trị.
Cục Quản lý Dược khẳng định, danh sách tiền kiểm sẽ tiếp tục được cập nhật và công bố định kỳ trong thời gian tới, bảo đảm tính minh bạch trong quản lý, đồng thời thể hiện quyết tâm của cơ quan chức năng trong việc siết chặt kiểm soát chất lượng thuốc lưu hành trên thị trường.
Thiên Trường