Theo đó,4 công ty dược sản xuất dược phẩm là Công ty cổ phần dược phẩm Tipharco, Công ty cổ phần dược Trung ương 3, Công ty cổ phần dược phẩm Trung ương 2, Công ty cổ phần BV Pharma. 4 công ty sản xuất dược phẩm không đạt tiêu chuẩn chất lượng, buộc thu hồi, tiêu hủy toàn bộ lô thuốc không đảm bảo chất lượng.
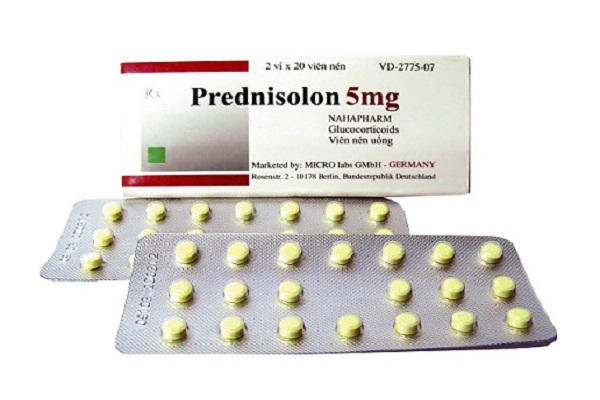 Công ty cổ phần dược phẩm Tipharco sản xuất thuốc viên nén Prednisolon 5mg không đạt tiêu chuẩn
Công ty cổ phần dược phẩm Tipharco sản xuất thuốc viên nén Prednisolon 5mg không đạt tiêu chuẩn
Công ty cổ phần dược phẩm Tipharco (Mỹ Tho, Tiền Giang) sản xuất thuốc viên nén Prednisolon 5mg, số đăng ký VD-13888-11, số lô 010317, hạn dùng 4.3.2020 không đạt tiêu chuẩn chất lượng mức độ 3 và buôn bán nguyên liệu làm thuốc Silymarin, số lô 20140912, hạn dùng 11.9.2017, đã hết hạn sử dụng.
Với 2 sai phạm trên, Cục Quản lý Dược đã xử phạt Công ty cổ phần dược phẩm Tipharco với tổng tiền là 130 triệu đồng. Cục Quản lý dược yêu cầu công ty phối hợp với các đơn vị liên quan thực hiện thu hồi và hủy toàn bộ lô thuốc không đạt chất lượng theo quy định. Cùng với đó, Cục Quản lý dược đã có hình thức xử phạt bổ sung là tước quyền sử dụng giấy chứng nhận đủ điều kiện kinh doanh thuốc đối với phạm vi nhập khẩu nguyên liệu làm thuốc trong thời gian 3 tháng đối với Công ty cổ phần dược phẩm Tipharco.
Công ty cổ phần dược phẩm Trung ương 2 (Hà Nội) và Công ty cổ phần BV Pharma (TPHCM) cùng bị xử phạt mức 70 triệu đồng do sản xuất thuốc không đạt chất lượng mức độ 2. Công ty cổ phần dược Trung ương 3 (Đà Nẵng) bị xử phạt thấp nhất, mức 40 triệu đồng do sản xuất thuốc Enalapril 10mg, SĐK:VD-15254-11, số lô 03/060818 không đạt tiêu chuẩn chất lượng mức độ 3.
Công ty cổ phần dược phẩm Trung ương 2 sản xuất thuốc Seared 4200IU, SĐK: VD-21906-14, số lô 00316, ngày sản xuất 9.12.2016, hạn dùng 9.6.2018; Sản phẩm của Công ty BV Pharma là thuốc Alphachymotrypsin BVP, SĐK: VD-13220-10, số lô 03B17, ngày sản xuất 27.2.2017, hạn dùng 27.2.2019.
Ngoài phạt tiền, Cục Quản lý dược đã yêu cầu thu hồi và tiêu huỷ toàn bộ sản phẩm, tước quyền sử dụng giấy chứng nhận điều kiện kinh doanh đối với 2 lại thuốc nói trên trong thời gian 3 tháng.
Đông Hòa