Trước đó, ngày 05/01, Hội đồng Tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc, Bộ Y tế có cuộc họp xem xét hồ sơ đề nghị cấp giấy đăng ký lưu hành thuốc chứa hoạt chất của các cơ sở sản xuất trong nước.
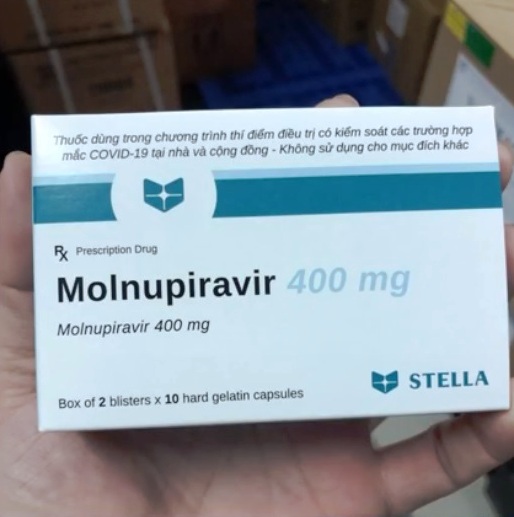
Tại cuộc họp, hội đồng đã xem xét một cách kỹ lưỡng, thận trọng các ý kiến thẩm định của các tiểu ban chuyên môn, các chuyên gia đầu ngành về tiêu chuẩn chất lượng, bào chế, dược lý lâm sàng và thống nhất đề xuất Bộ Y tế cấp giấy đăng ký lưu hành có điều kiện cho 3 thuốc chứa hoạt chất Molnupiravir, thuốc thuốc kháng virus có chỉ định điều trị Covid-19. Đồng thời, các cơ sở sản xuất thuốc phải đảm bảo các điều kiện cụ thể để kiểm soát chặt chẽ chất lượng thuốc sau khi được cấp giấy đăng ký lưu hành.
Cụ thể, doanh nghiệp phải thực hiện kiểm tra chất lượng nguyên liệu đạt yêu cầu trước khi sản xuất; theo dõi, kiểm tra chất lượng thuốc hằng tháng sau khi được cấp giấy đăng ký lưu hành và báo cáo cơ quan quản lý để giám sát chặt chẽ về chất lượng, tuổi thọ của thuốc; tiếp tục thực hiện nghiên cứu độ ổn định của thuốc và nộp dữ liệu nghiên cứu, hồ sơ cập nhật hạn dùng để thẩm định theo hướng dẫn và yêu cầu của bộ hồ sơ kỹ thuật chung ASEAN.
Bộ Y tế cũng yêu cầu các cơ quan quản lý và đơn vị chuyên môn kiểm soát chặt chẽ về chất lượng và giá theo đúng quy định của Luật Dược, chống mọi biểu hiện tiêu cực, lợi ích nhóm trong quá trình sản xuất và lưu hành thuốc.
Sau khi hãng dược Merch nhượng quyền sản xuất thuốc điều trị Covid-19 có hoạt chất Molnupiravir, có khoảng 10 công ty dược trong nước đã nộp hồ sơ đăng ký sản xuất thuốc điều trị Covid-19. Tuy nhiên, đến hôm nay mới chỉ có 03 doanh nghiệp đủ điều kiện cấp phép lần này.
Molravir 400 được chỉ định cho người trên 18 tuổi, với liều 400mg uống 2 lần mỗi ngày trong vòng 05 ngày.
Q.N (t/h)