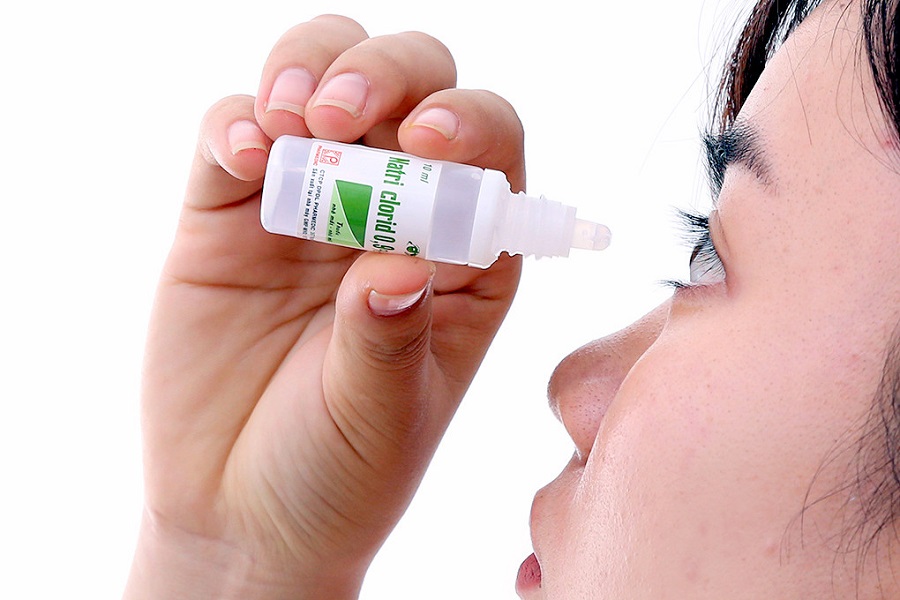
Số công bố tiêu chuẩn thiết bị y tế do doanh nghiệp tự công bố bị thu hồi tăng đột biến
Những con số 70, 190, rồi hàng trăm số công bố tiêu chuẩn do doanh nghiệp tự công bố bị thu hồi trong thời gian qua đang như một “bản kiểm điểm” cho ngành Y tế. Thực trạng này, đang để lại những dư âm vô cùng nặng nề: Bác sĩ thêm phần áp lực, bệnh viện thêm lúng túng, còn bệnh nhân thì phập phồng với nỗi lo vô hình ngay trên giường bệnh.
Cụ thể, chỉ tính riêng tháng 6/2025, Sở Y tế Hà Nội đã thu hồi 415 số công bố tiêu chuẩn áp dụng đối với thiết bị y tế (TBYT) thuộc loại A, B không đạt.
Trước đó, trong tháng 5/2025, Sở Y tế Hà Nội đã ban hành hai quyết định, rút lại 70 số công bố thiết bị y tế loại A, B. Lý do thu hồi: Sản phẩm không phù hợp định nghĩa TBYT, mục đích sử dụng sai phân loại, căn cứ theo Nghị định 98/2021/NĐ-CP và Công văn 2098/BYT-TB-CT.

Chỉ sau 2 tháng (tháng 7/2025) Sở Y tế Hà Nội tiếp tục ban hành quyết định thu hồi 190 số công bố tiêu chuẩn áp dụng cho các sản phẩm được phân loại TBYT loại A và B. Lý do thu hồi là các sản phẩm “không phù hợp với định nghĩa TBYT”. Không dừng lại ở đó, nhiều đơn vị còn bị phát hiện làm thủ tục công bố sai quy định, vi phạm quy trình quản lý. Điều này đồng nghĩa rằng những sản phẩm vốn không đủ chuẩn, vẫn được phép tràn vào bệnh viện, nhà thuốc, thậm chí ngay trong tủ thuốc của từng gia đình.
Với số công bố tiêu chuẩn do doanh nghiệp tự công bố “khổng lồ” bị thu hồi nêu trên, cho thấy, tình trạng này không còn là ngẫu nhiên, “chợt đến chợt đi”, mà phản ánh thực trạng của dấu hiệu kéo dài, vi phạm có hệ thống.
Trong 190 số bị thu hồi này, có không ít doanh nghiệp bị rút tới hàng chục bị giấy công bố sản phẩm. Đơn cử, như: Công ty cổ phần Dược liệu Bảo Sâm dẫn đầu với 20 sản phẩm bị rút giấy công bố, từ xịt họng, nước súc miệng, xịt mũi, xịt tai; Công ty TNHH Đông Dược Phúc Cường và Công ty cổ phần Dược phẩm Elaphe mỗi nơi có 8 sản phẩm bị loại, bao gồm xịt khớp, dung dịch nhỏ tai, thuốc nhỏ mắt, nước muối sinh lý đa năng, cồn y tế 90 độ; Công ty TNHH Dược phẩm V&S Việt Nam mất 7 số công bố.
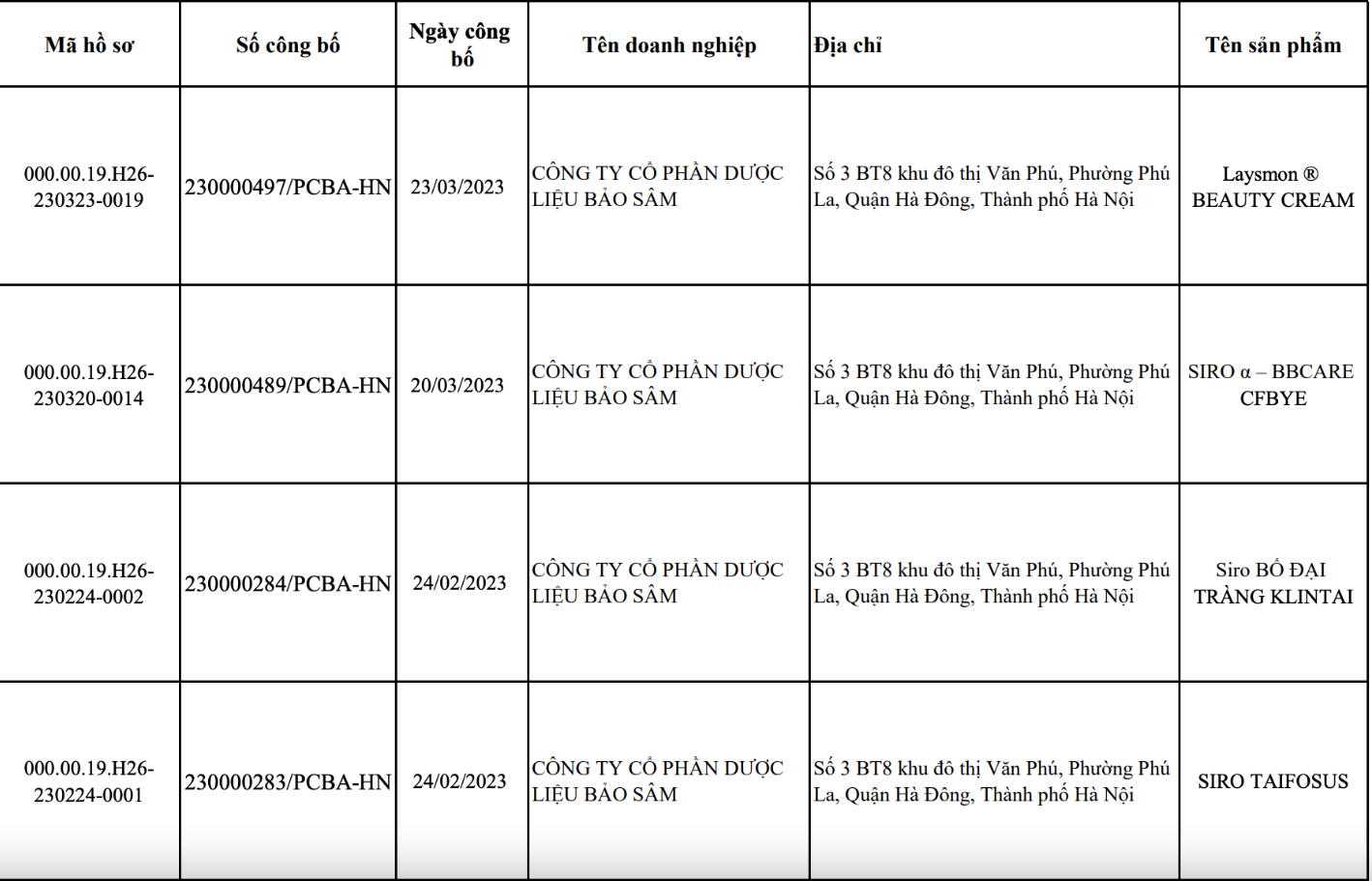
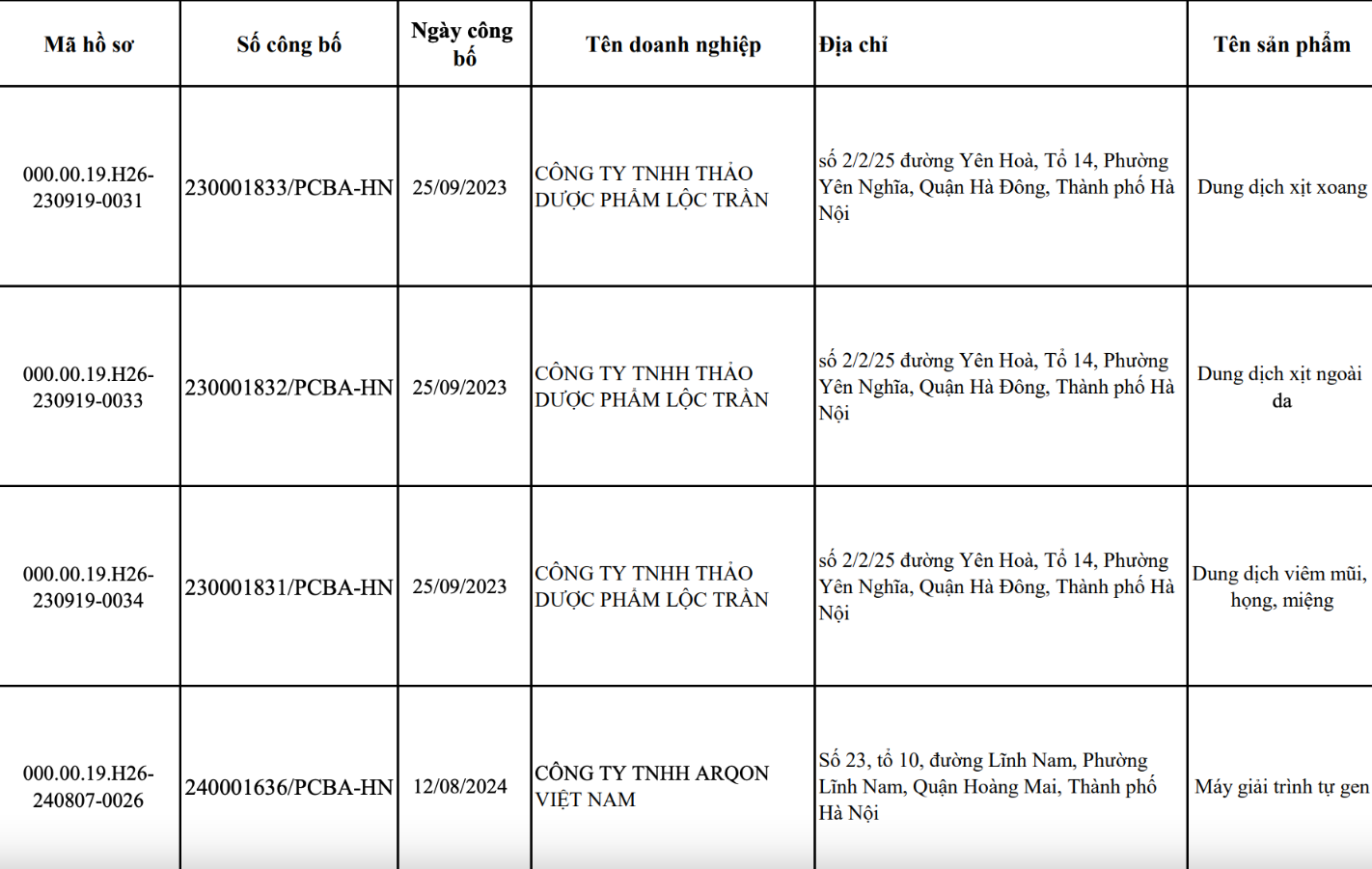
Ngoài ra, các Công ty cổ phần Công nghệ Dược Mỹ phẩm Hà Nội, Công ty TNHH Vật tư Trang thiết bị Y tế Hà Anh, Công ty TNHH Liên doanh Hungari - Việt Nam và Công ty TNHH Dược phẩm & Trang thiết bị Y tế Phú Minh Khang đều bị rút 5 sản phẩm…
Trong số các đơn vị này, những cái tên tưởng như quen thuộc với đông đảo người tiêu dùng, như: Hà Anh - đơn vị từng cung cấp các bộ dụng cụ bơm xi măng cột sống, bộ dụng cụ phẫu thuật, kim chọc cột sống, hệ thống máy khoan đa năng, những thiết bị liên quan trực tiếp đến ca mổ. Hay, liên doanh Hungari - Việt Nam với các sản phẩm xịt giảm đau, dung dịch vệ sinh phụ nữ. Nhiều doanh nghiệp khác, như HAMO-PHAR, NCK FARMACY (Thanh Xuân), Dược phẩm Bình Minh, ODOGROUP, EU Việt Nam mỗi đơn vị bị rút 4 số; Ngân Hà, Thành Phát mỗi nơi 3 số.
Thậm chí, ngay cả các doanh nghiệp lâu năm, như: Hóa dược TW8, TW9, hay các đơn vị phân phối như Medstand, Sun For Life, KYH Bio Tech Việt Nam, Healthcare HCT, Khôi Nguyên cũng góp mặt trong “bảng danh dự”. Ngay cả Viện Nghiên cứu các bài thuốc dân tộc Việt Nam cũng bị “nêu tên” với 5 số công bố gồm gel, kem bôi, xịt xoang, xịt mũi… Điều này cho thấy, sai phạm không chỉ là “chuyện riêng” của các doanh nghiệp thương mại, mà đang len lỏi vào cả các các đơn vị nghiên cứu.
Những sản phẩm phổ biến, dễ sử dụng, tưởng chừng vô hại, như: Nước muối sinh lý, cồn y tế, xịt mũi họng, xịt khớp, gel giảm đau, máy đo đường huyết, bộ xét nghiệm HIV, xét nghiệm cúm…, nhưng khi được “dán nhãn” TBYT sai bản chất, thì hệ lụy mang lại không còn đơn giản nữa. Bởi, một ống xịt mũi kém chất lượng có thể gây viêm nhiễm, một bộ xét nghiệm HIV sai lệch, có thể thay đổi cả cuộc đời người bệnh.
Lợi dụng cơ chế tự công bố, hạ mức rủi ro để dễ trúng thầu
Ngoài ra, thời gian qua, không ít nhà thầu phản ánh tình trạng TBYT phân loại sai mức độ rủi ro nhưng vẫn dự thầu, trúng thầu. Nhiều chủ đầu tư/bên mời thầu cho biết, không có đủ cơ sở pháp lý để loại nhà thầu, trừ khi TBYT đó bị thu hồi, hoặc không có thông tin đăng ký được công bố trên Hệ thống do Bộ Y tế quản lý.
Đơn cử, ngày 10/7 vừa qua Sở Y tế TP. Hồ Chí Minh cho biết, qua rà soát cơ quan này phát hiện, một số cơ sở sản xuất, nhập khẩu TBYT đã lợi dụng cơ chế tự công bố để hạ thấp mức độ rủi ro, phân loại thiết bị y tế nhằm dễ dàng được công bố hoặc trúng thầu.
Cụ thể, Sở Y tế TP. Hồ Chí Minh đã tiến hành kiểm tra 226 cơ sở, bao gồm: 6 cơ sở mỹ phẩm, 80 cơ sở dược, 121 cơ sở sản xuất, kinh doanh TBYT, 19 cơ sở khám chữa bệnh. Kết quả, 41 cơ sở vi phạm và bị xử lý với tổng số tiền phạt hơn 2,2 tỷ đồng; buộc nộp lại trị giá tang vật vi phạm (mỹ phẩm) hơn 39,7 triệu đồng...
Bên cạnh đó, Phòng Y tế quận/huyện (cũ) cũng đã tiến hành kiểm tra 1.059 cơ sở hành nghề y, dược trên địa bàn quản lý; tiến hành xử lý 14 cơ sở, với tổng số tiền phạt hơn 169 triệu đồng.
Đối với lĩnh vực TBYT, Sở Y tế TP. Hồ Chí Minh cũng đã ban hành 17 quyết định thu hồi với 364 số công bố tiêu chuẩn áp dụng đối với các sản phẩm được phân loại TBYT loại A và B. Trong đó, nhiều sản phẩm bị công bố sai như: gel rửa tay, máy đo đường huyết, máy massage, dung dịch rửa phụ khoa, dụng cụ chăm sóc tai mũi họng…
Qua kiểm tra, Sở Y tế TP Hồ Chí Minh ghi nhận các lỗi thường gặp của các doanh nghiệp như: Sản phẩm không phù hợp với định nghĩa là thiết bị y tế; phân loại TBYT không đúng quy định, phân loại sai hoặc tự hạ thấp mức độ rủi ro của TBYT; thành phần hồ sơ tự công bố chưa đúng quy định, thông tin hồ sơ không chính xác…
Nếu đi sâu vào hồ sơ tự công bố, rất dễ để nhận thấy đủ các loại “chiêu trò”. Từ các sản phẩm vốn là mỹ phẩm (dầu gội, sữa tắm, sữa rửa mặt), thuốc cổ truyền, thực phẩm chức năng lại được khai là thiết bị y tế. Các xét nghiệm in vitro có rủi ro cao như: HIV, HBV, HCV… lẽ ra phải được phân loại khắt khe, chặt chẽ…, thì lại bị xếp vào nhóm A, B để dễ thông qua…
Bên cạnh đó, thành phần hồ sơ thì thiếu đủ thứ. Từ giấy lưu hành tự do (CFS) cho hàng nhập khẩu, đến phiếu tiếp nhận hồ sơ cho hàng trong nước, chứng nhận ISO 13485, bằng chứng về kho bảo quản, phương tiện vận chuyển. Thậm chí, có cả những giấy chứng nhận ISO từ tổ chức không đủ thẩm quyền, văn bằng chuyên môn không hợp lệ, kết quả kiểm nghiệm không từ cơ sở đủ năng lực. Thậm chí có trường hợp, còn sử dụng cả giấy ủy quyền, giấy bảo hành không hợp pháp hóa lãnh sự…
Cần đảm bảo an toàn cho người bệnh và hệ thống y tế Quốc gia
Theo Sở Y tế Hà Nội cho biết, thời gian qua cơ quan này luôn chú trọng, đẩy mạnh ứng dụng công nghệ thông tin; xây dựng cơ sở dữ liệu quốc gia về thiết bị y tế, công khai thông tin về sản phẩm, số công bố, kết quả kiểm tra; ứng dụng mã QR code để truy xuất nguồn gốc sản phẩm; thực hiện hiệu quả công tác quản lý chất lượng bệnh viện và an toàn người bệnh, nhân viên y tế.
Thông tin trước báo chí, TS Nguyễn Đình Hưng cho biết, Sở Y tế Hà Nội đã nâng cao năng lực, đẩy mạnh cải tiến chất lượng chuyên môn cho toàn hệ thống thông qua đầu ngành quản lý chất lượng; hướng dẫn xây dựng và chuẩn hóa các quy trình, tiêu chuẩn chất lượng để các đơn vị áp dụng. Bên cạnh đó, Sở Y tế Hà Nội cũng tăng cường ứng dụng công nghệ thông tin; thực hiện giám sát và đánh giá thường xuyên mức độ cải tiến chất lượng cho các bệnh viện, giúp bệnh viện tìm ra những lỗ hổng, khoảng trống…
Tuy nhiên, thực tế cho thấy, khoảng cách giữa văn bản và thực tiễn còn rất xa vời. Bởi, người bệnh không thể an tâm chỉ bằng một mã QR, hay báo cáo treo tường. Mà cái họ cần, là tận mắt chứng kiến các thiết bị trong phòng mổ thực sự an toàn, đáng tin cậy.
Theo Nghị định 07/2023/NĐ-CP, các thiết bị y tế đã bán cho cơ sở y tế hoặc người sử dụng vẫn tiếp tục dùng đến khi hết hạn hoặc bị thanh lý, trừ khi lỗi không thể khắc phục. Về quản lý, cách xử lý này nhằm tránh lãng phí. Nhưng, với người bệnh, lại trở thành một nỗi bất an. Bởi, ai dám chắc sản phẩm đã bị “gạch tên” trên giấy, không tiềm ẩn rủi ro trên giường bệnh? Và nếu sự cố xảy ra, thì ai sẽ chịu trách nhiệm?
Liên quan đến vấn đề này, Luật sư Vi Văn Diện, Giám đốc Công ty Luật Thiên Minh nhận định: Theo quy định tại Thông tư số 05/2022/TT-BYT ngày 1/8/2022 của Bộ Y tế, việc phân loại TBYT được thực hiện theo nguyên tắc dựa trên mức độ rủi ro tiềm ẩn liên quan đến việc sử dụng thiết bị đối với cơ thể người. Có bốn nhóm chính: loại A (rủi ro thấp), loại B (rủi ro trung bình thấp), loại C (rủi ro trung bình cao) và loại D (rủi ro cao nhất).
Ngoài Thông tư 05, việc quản lý trang TBYT còn được điều chỉnh bởi Nghị định số 98/2021/NĐ-CP ngày 8/11/2021 của Chính phủ, và Nghị định số 07/2023/NĐ-CP. Theo đó, thiết bị y tế loại C và D (có mức độ rủi ro cao hơn) khi lưu hành phải trải qua các thủ tục nghiêm ngặt hơn như: thẩm định hồ sơ công bố, báo cáo thử nghiệm, hoặc đánh giá sự phù hợp bởi tổ chức được Bộ Y tế công nhận.
“Tuy nhiên, để rút ngắn thời gian và chi phí, nhiều doanh nghiệp cố tình khai báo thiết bị loại C/D thành B hoặc A, nhờ đó được “miễn” các bước kiểm định hoặc chứng nhận bắt buộc. Việc khai báo sai loại thiết bị để né kiểm định là hành vi không thể xem nhẹ, bởi nó không chỉ phá vỡ nguyên tắc quản lý rủi ro y tế mà còn đặt người dân vào tình trạng sử dụng các thiết bị chưa được thẩm định đầy đủ.
Đây là hành vi cần bị lên án và xử lý nghiêm minh nhằm bảo đảm tính nghiêm túc, minh bạch và an toàn trong hoạt động kinh doanh TBYT tại Việt Nam. Có thể bị xử lý hành chính theo Nghị định 117/2020/NĐ-CP, thậm chí bị thu hồi số lưu hành thiết bị y tế hoặc truy cứu trách nhiệm hình sự nếu gây hậu quả nghiêm trọng...”, Luật sư Diện phân tích.

Cũng theo Luật sư Vi Văn Diện, trên thực tế nhiều hồ sơ tự công bố TBYT đã bị phát hiện có nội dung không đầy đủ, không đúng định nghĩa thiết bị y tế theo quy định tại khoản 1 Điều 2 Nghị định 98/2021/NĐ-CP. Một số sản phẩm không phải là TBYT, nhưng vẫn được “gắn mác” để hưởng chính sách ưu đãi, thậm chí né tránh các quy trình cấp phép nghiêm ngặt, gây ảnh hưởng tiêu cực đến thị trường và người tiêu dùng.
Ngoài nguy cơ trực tiếp đối với người sử dụng, việc đưa thiết bị loại C/D ra thị trường dưới mác loại B để né thủ tục còn phá vỡ nguyên tắc quản lý rủi ro y tế của Nhà nước, khiến cơ quan quản lý không thể kiểm soát chất lượng thực tế của TBYT lưu hành. Điều này không chỉ ảnh hưởng đến uy tín hệ thống y tế mà còn làm gia tăng chi phí xử lý sự cố, khiếu kiện và rủi ro pháp lý về sau…
“Chính vì vậy, quy trình kiểm định, thẩm định đối với thiết bị y tế nhóm C và D là yêu cầu bắt buộc nhằm đảm bảo an toàn cho người bệnh, hiệu quả điều trị và bảo vệ hệ thống y tế quốc gia trước các rủi ro tiềm ẩn từ thị trường TBYT đạt chuẩn.
Trong trường hợp xảy ra tai biến y khoa, hoặc hậu quả do TBYT không đạt chuẩn gây ra, trách nhiệm có thể được xác định đối với cả doanh nghiệp cung cấp thiết bị và cơ sở y tế sử dụng, tùy theo mức độ vi phạm, mối liên hệ nhân quả và hành vi cụ thể của từng bên…”, luật sư Vi Văn Diện cho biết thêm.
Tuấn Ngọc