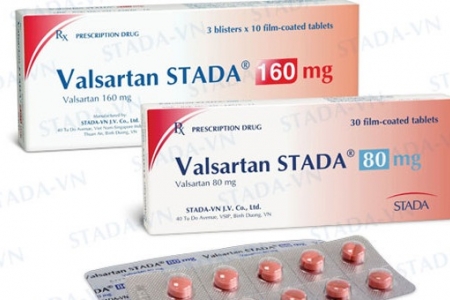
Tuy nhiên, việc đình chỉ lưu hành chỉ áp dụng với 23 thuốc có sử dụng nguyên liệu Valsartan do Công ty Zhejiang Huahai Pharmaceuticals của Trung Quốc sản xuất. Nhằm bảo đảm cung ứng đủ thuốc có chất lượng phục vụ nhu cầu điều trị và tránh biến động về giá thuốc, Bộ Y tế yêu cầu các cơ sở sản xuất, kinh doanh tiếp tục nhập khẩu, sản xuất, lưu hành 88 thuốc còn lại chứa Valsartan không sử dụng nguyên liệu của Công ty Zhejiang Huahai Pharmaceuticals.
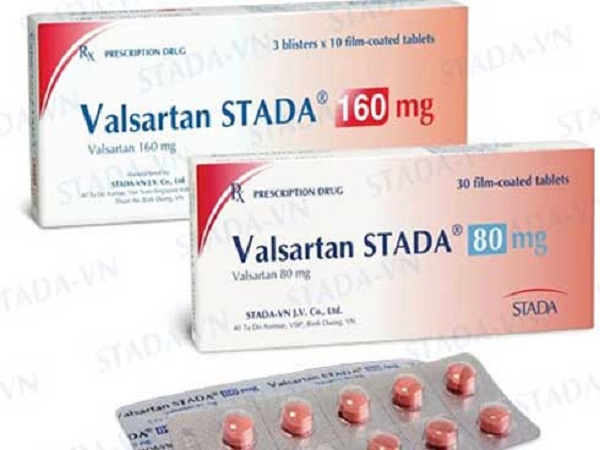
1 trong 23 thuốc điều trị tim mạch có nguy cơ gây ung thư
Được biết, dược chất Valsartan được dùng để điều trị bệnh tăng huyết áp và suy tim, ngăn ngừa đột quỵ cho người cao tuổi, nhồi máu cơ tim và các vấn đề về thận. Cơ quan Quản lý dược phẩm châu Âu (EMA), cơ quan Quản lý dược Canada và một số nước thông báo về việc thu hồi số thuốc chứa Valsartan do Công ty Zhejiang Huahai Pharmaceuticals của Trung Quốc sản xuất, có chứa tạp chất nguy cơ gây ung thư.
Cùng ngày, Bộ Y tế có thông cáo báo chí liên quan đến việc một số phương tiện thông tin đại chúng đưa tin về vắc xin phòng bệnh dại ở người và vắc xin DPT (phòng bệnh bạch hầu - ho gà - uốn ván) do Công ty Changsheng Biotechnology, trụ sở ở TP Trường Xuân, tỉnh Cát Lâm, Trung Quốc bị phát hiện vi phạm các tiêu chuẩn trong sản xuất vắc xin và đã bị cơ quan Quản lý dược phẩm Trung Quốc thu hồi giấy phép sản xuất, đồng thời tiến hành điều tra hình sự. Sau khi kiểm tra và rà soát việc cấp giấy đăng ký lưu hành, giấy phép nhập khẩu vắc xin, đến nay chưa có sản phẩm vắc xin phòng bệnh dại ở người và vắc xin DPT do Công ty Changsheng Biotechnology, Trung Quốc sản xuất hoặc cung cấp được Bộ Y tế cấp giấy đăng ký lưu hành, giấy phép nhập khẩu để lưu hành tại Việt Nam.
Bảo Ngọc